Идеал газ заңы (Менделеев-Клапейрон теңдеуі)
Gas Properties by PhET Interactive Simulations, University of Colorado Boulder, licensed under CC-BY-4.0 (https://phet.colorado.edu)
Жобаның атауы: Идеал газ заңы (Менделеев-Клапейрон теңдеуі)
Бұл виртуалды зертхана келесі тақырыптар бойынша химия сабақтарында пайдалануға арналған:
- 10 сынып. VI тарау. «Кинетика».
Мақсаты:
- Gas properties интерактивті PhET симуляциясы арқылы Идеал газ Заңын зерттеу
- Бойль, Шарль және Гей-Люссак заңдарынан идеал газ заңын (PV = nRT) түсіну үшін қатынастарды біріктіру.
Теориялық бөлім
Газ заңдары газдардың әртүрлі жағдайлардағы әрекетін сипаттайды. Бұл заңдарды түсіну газдардың үш макроскопиялық шамалардың (қысымның, көлемнің немесе температураның) өзгеруіне қалай әсер ететінін болжауға көмектеседі.
Идеал газ заңы
Идеал газ заңы, Менделеев-Клапейрон теңдеуі деп те аталады, бірнеше қарапайым газ заңдарын бір теңдеуге біріктіреді:
PV = nRT
Бұл теңдеу қысымның (P), көлемнің (V), бөлшектердің санының (n), газ тұрақтысының (R) және температураның (T) өзара байланысын көрсетеді.
- P (қысым) — газ бөлшектерінің өз ыдысының қабырғаларына түсіретін күші.
- V (көлем) — бұл газ орын алатын кеңістік.
- n (моль саны) — газ молекулаларының саны.
- R (газ тұрақтысы) — өлшем бірліктерін дұрыс (8,31 Дж/(моль·К)) ететін тұрақты мән.
- T (температура) — газ бөлшектерінің қозғалу жылдамдығының өлшемі.
Бойль заңы (Тұрақты T кезінде P ∝ 1/V)
Бойль заңы тұрақты температурада газдың қысымы мен көлемі кері пропорционал болатынын айтады. Бұл дегеніміз:
- Көлем азайған сайын қысым күшейеді.
- Көлем ұлғайған сайын қысым төмендейді.
Теңдеу: P₁V₁ = P₂V₂
Шарль заңы (тұрақты Р кезінде V ∝ T)
Шарль заңы тұрақты қысымда газдың көлемі мен температурасы тура пропорционал болатынын айтады. Бұл дегеніміз:
- Температура жоғарылаған сайын көлем ұлғаяды.
- Температура төмендеген сайын көлем азаяды.
Теңдеу: V₁/T₁ = V₂/T₂
Гей-Люссак заңы (тұрақты V кезінде P ∝ T)
Гей-Люссак заңы тұрақты көлемде газдың қысымы мен температурасы тура пропорционал болатынын айтады. Бұл дегеніміз:
- Температура жоғарылаған сайын қысым жоғарылайды.
- Температура төмендеген сайын қысым төмендейді.
Теңдеу: P₁/T₁ = P₂/T₂
Тәжірибелік бөлім

- Симуляцияны іске қосыңыз. Бұл құрал контейнердегі газ бөлшектерінің әрекетін бақылауға мүмкіндік береді, қысым, көлем және температура сияқты шамаларды түсінуге көмектеседі.
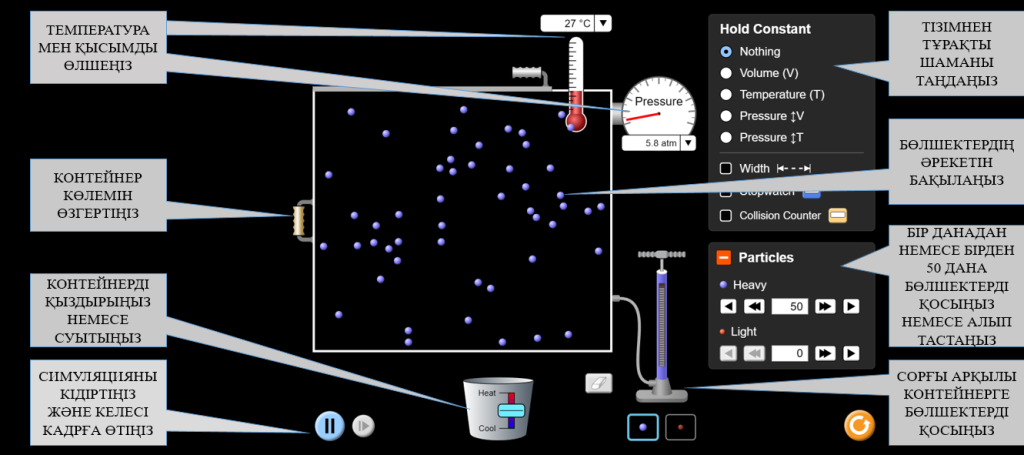
2. Симуляцияның құрамдас бөліктерімен танысыңыз: бөлшектер жүйесі (газ молекулалары), контейнер және қысым (P), көлем (V) және температура (T) сияқты реттелетін параметрлер.
Бойль заңын зерттеу (тұрақты Т үшін P ∝ 1/V)
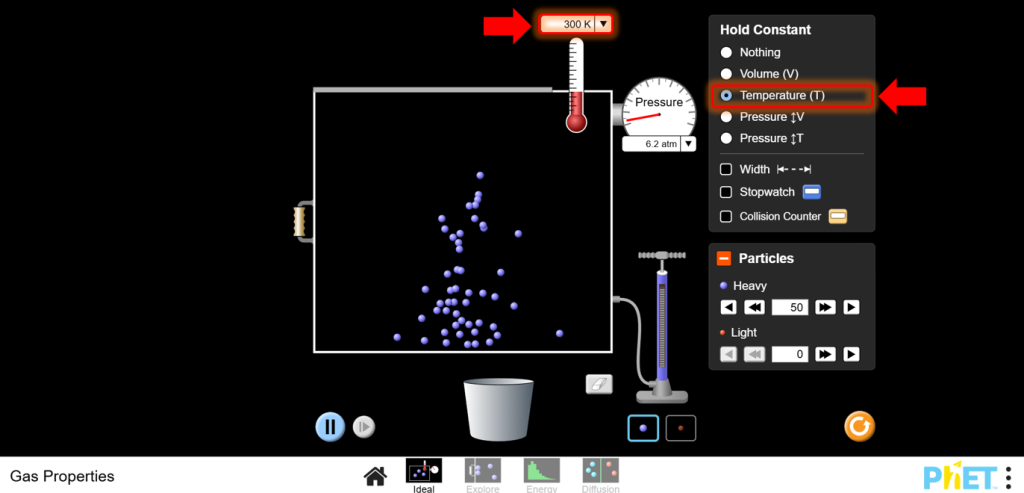
- Симуляциядағы Ideal режиміне өтіңіз.Бастапқы шамаларды орнатыңыз: Бөлшектердің белгіленген санынан (N) және тұрақты температурадан (T) бастаңыз. Сіз қысымның көлемге байланысты қалай өзгеретінін байқайсыз.
4. Көлем шамасын реттеңіз:
a.Көлемді өзгерту үшін контейнердің сол жақ қабырғасын пайдаланыңыз.Көлемді азайтыңыз және қысымның жоғарылауын бақылаңыз.
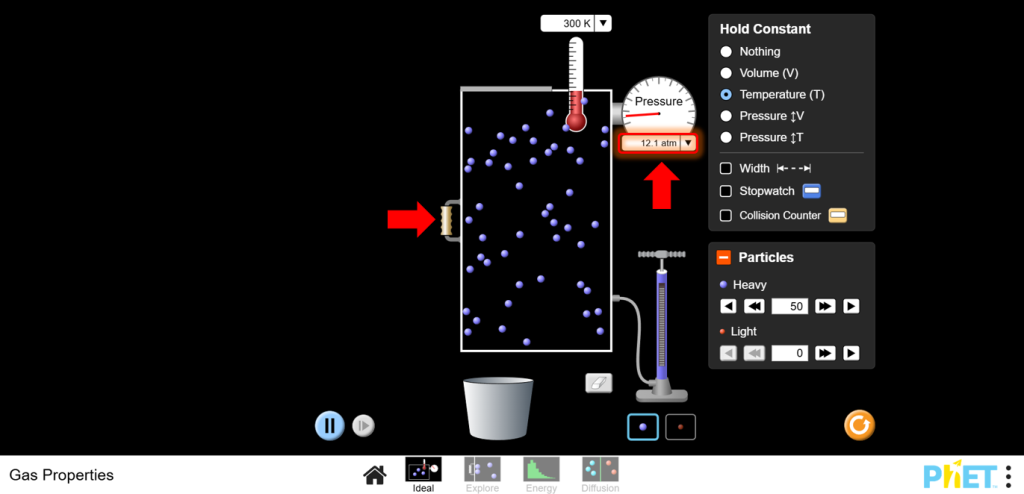
b. Көлемді арттырыңыз және қысымның төмендеуін бақылаңыз.
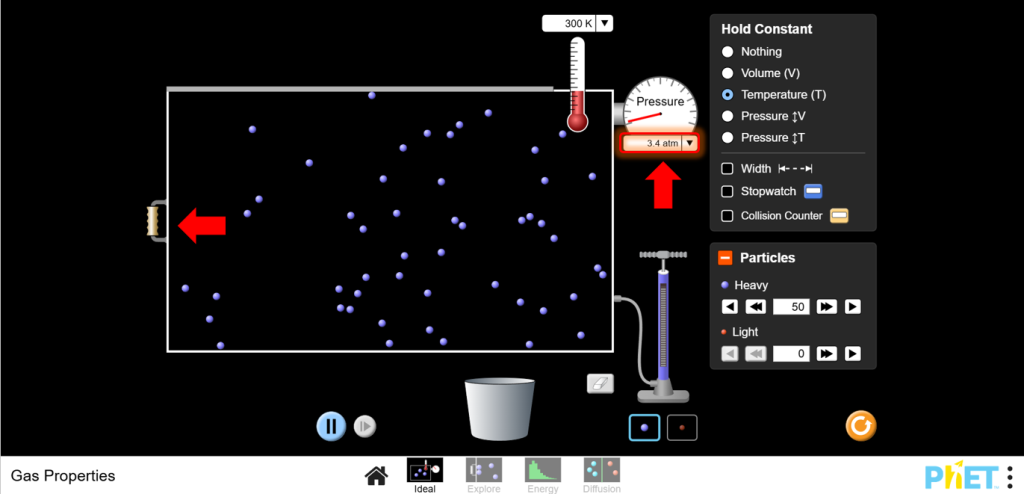
5. Бойль заңы тұрақты температурада қысым мен көлем кері пропорционал екенін айтады. Бақылауларыңызды жазып алыңыз және кері байланысты көру үшін Р-ның 1/V-ге қатысты графигін салыңыз.
Шарль заңын зерттеу (тұрақты Р кезінде V ∝ T)
- Шарль заңының параметрі:Ideal режиміне өтіңіз. Қажет болса, контейнердің сол жақ қабырғасын реттеу арқылы қысымды тұрақты ұстаңыз.
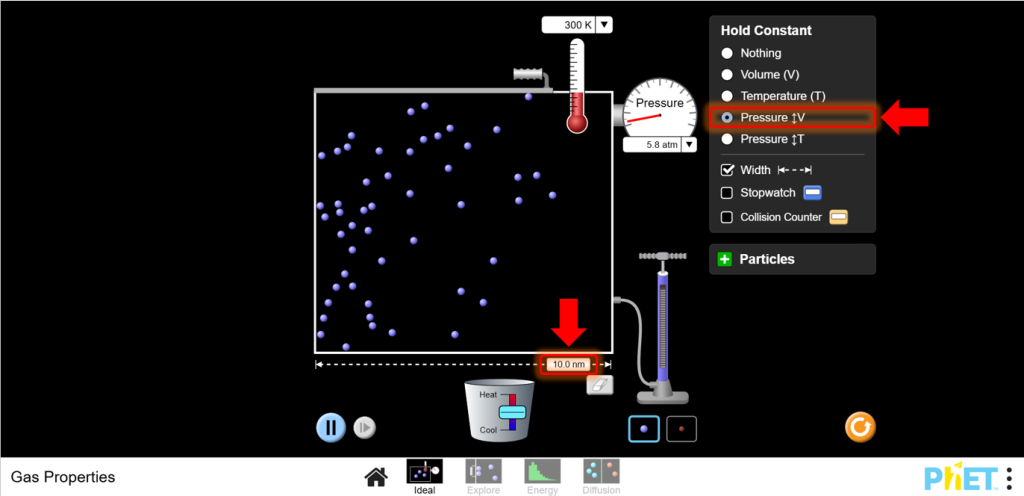
7. Температураны өзгертіңіз:
a. Қыздырғыштың көмегімен температураны арттырыңыз. Ыдыстың көлемі температураға байланысты қалай өзгеретініне назар аударыңыз. Температура жоғарылаған сайын көлемнің ұлғаятынына және назар аударыңыз.
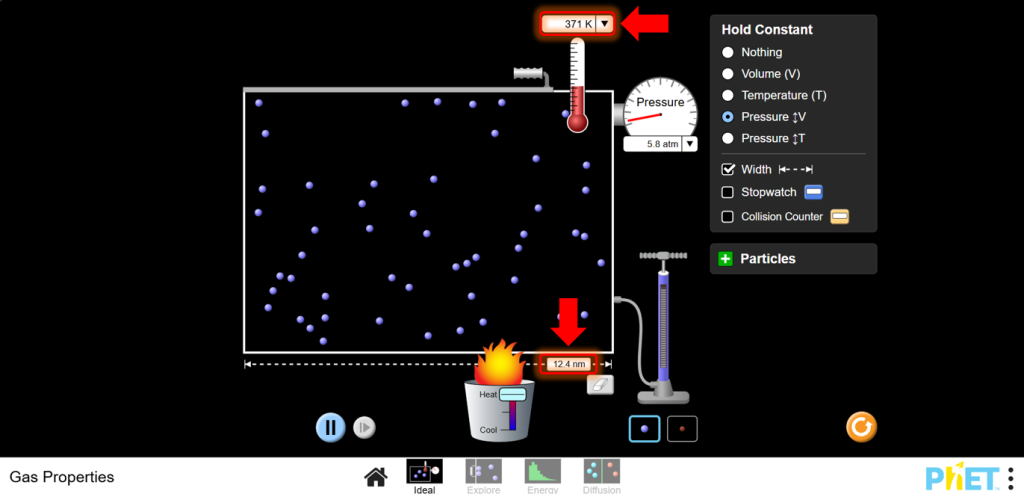
b. Суытқыштың көмегімен температураны төмендетіңіз. Температура төмендеген сайын көлемнің азаятынына назар аударыңыз.
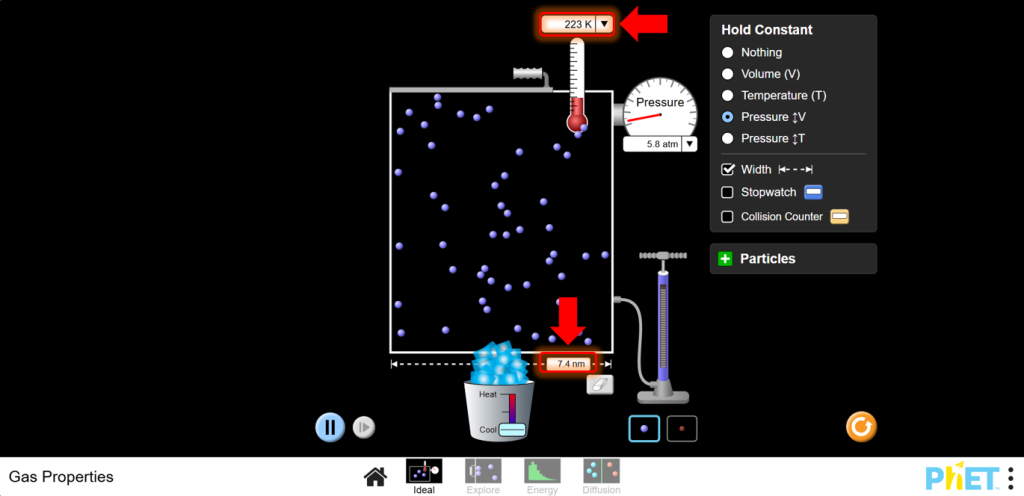
8.Шарль заңы тұрақты қысымдағы температура мен көлем арасындағы тікелей байланысты көрсетеді. V-нің T-ға қатысты графигін тұрғызыңыз және сызықтық байланысты бақылаңыз.
Гей-Люссак заңын зерттеу (тұрақты V кезінде P ∝ T)
- Гей-Люссак заңының параметрі:Ideal режимінде жұмысты жалғастырыңыз.Контейнер көлемін өзгертпей, тұрақты ұстаңыз.
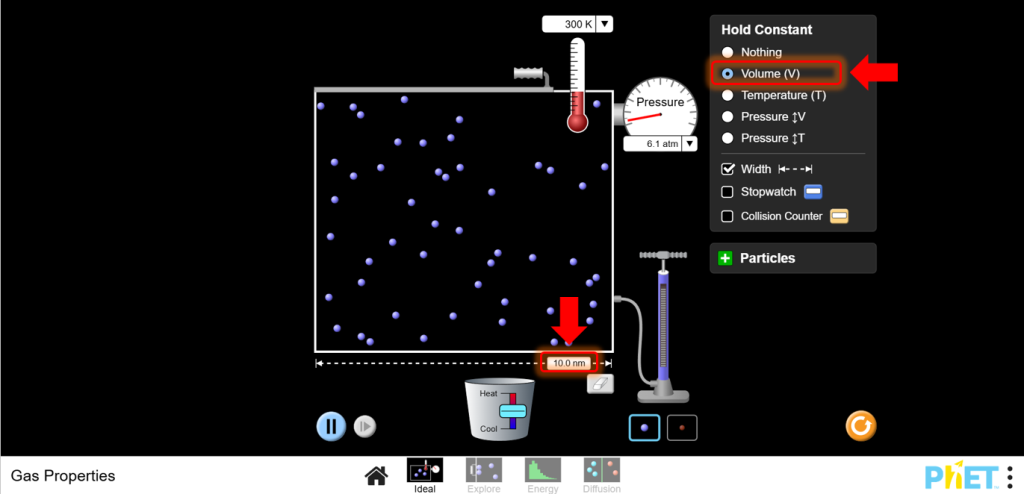
10.Температураны өзгертіңіз:
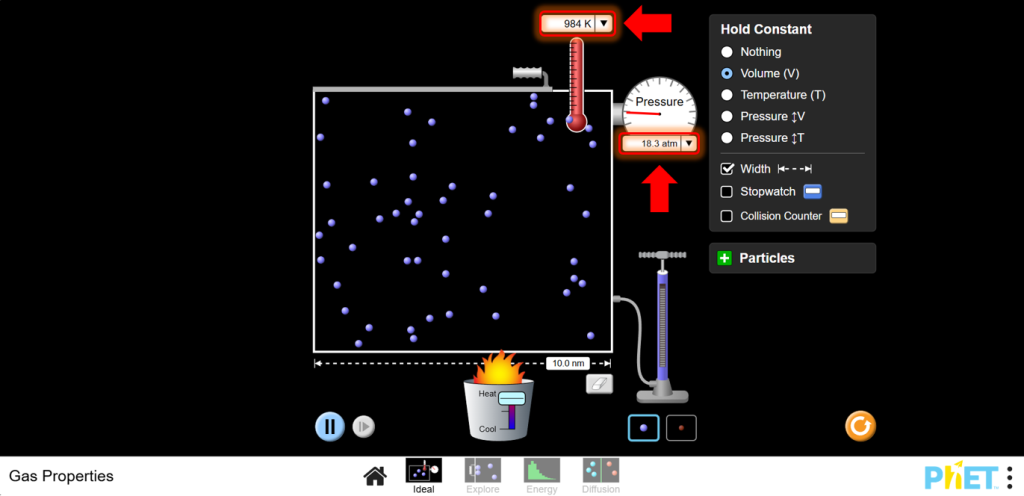
a. Температураны арттыру үшін жылытқышты пайдаланыңыз. Температура өзгерген кезде қысымның қалай өзгеретінін қадағалаңыз. Сіз температураның жоғарылауымен қысымның жоғарылайтынын көресіз.
b.Температураны төмендету үшін суытқышты пайдаланыңыз. Сіз температураның төмендеуімен қысымның да төмендейтін көресіз.
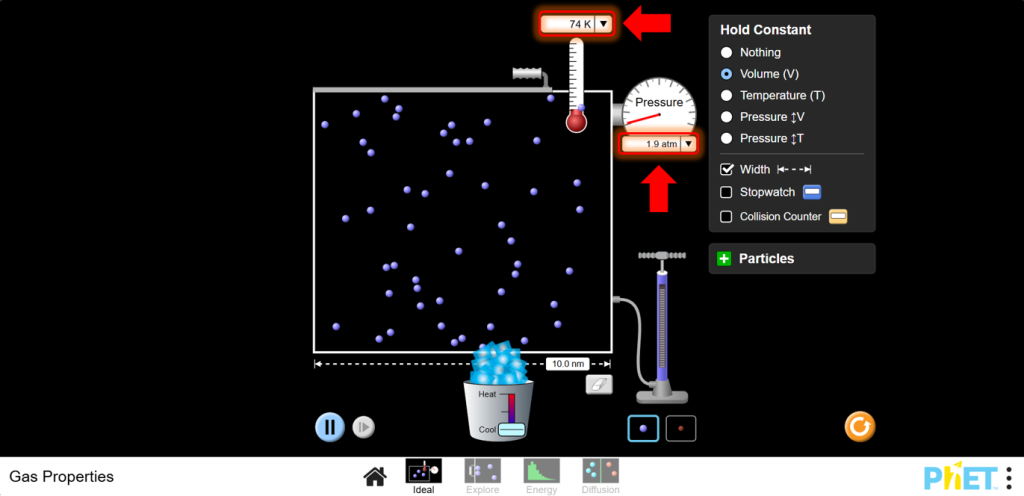
11. Гей-Люссак заңы тұрақты көлемдегі қысым мен температура арасындағы тікелей байланысты бекітеді. Осы тура пропорционалдылықты елестету үшін Р-ның Т-ға қатысты графигін салыңыз.
Идеал газ заңын қолдану (PV = nRT)
- Бойль, Шарль және Гей-Люссак заңдары идеалды газ заңына қалай біріктірілетінін зерттеп көріңіз.
- Тәжірибе жасаңыз:
a. Бөлшектердің бекітілген санын таңдаңыз.
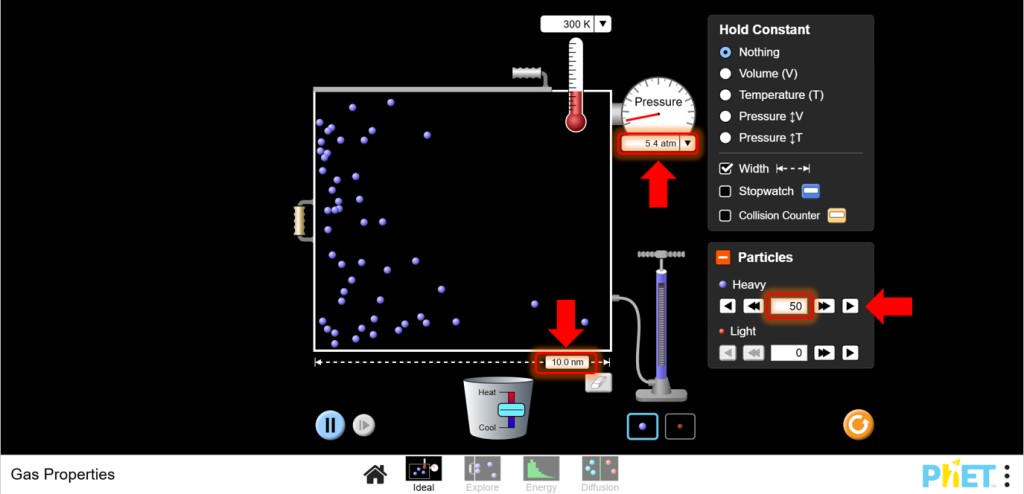
b. Бір айнымалыны (мысалы, көлемді) реттеңіз және қысым мен температураның өзгеруін бақылаңыз. Идеал газ заңы негізінде өзгерістерді болжаңыз
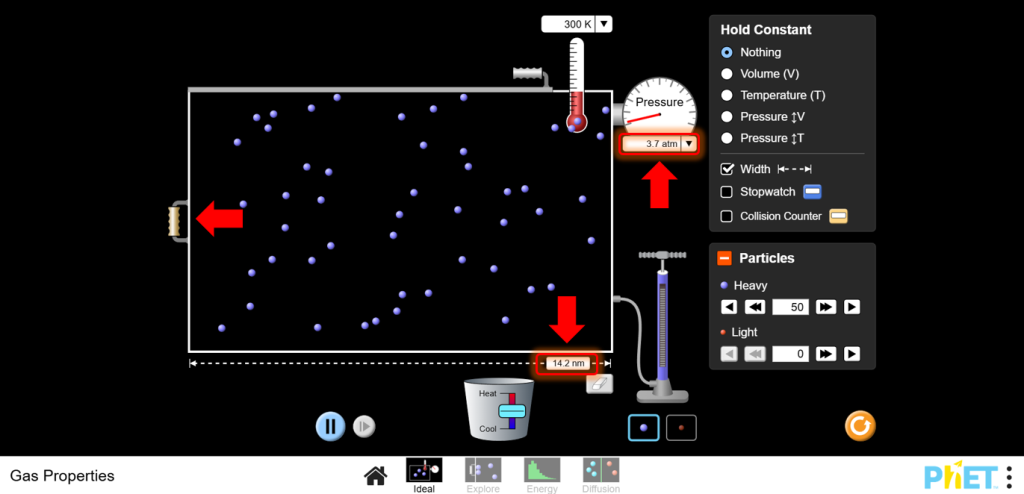
14. Математикалық байланысты нығайта отырып, PV = nRT көмегімен белгісіз шамаларды есептеу үшін әртүрлі сценарийлермен жұмыс істеуге болады.
Қорытынды
«Gas Properties» PhET симуляциясын пайдалану идеал газ заңын және оның құрамдас бөліктерін: Бойль, Шарль және Гей-Люссак заңдарын зерттеуге мүмкіндік берді. Интерактивті тәжірибелер жүргізу арқылы оқушылар әртүрлі жағдайларда газдардың әрекетін бақылауға және түсінуге мүмкіндік алды. Симуляция оқушыларға теориялық тұжырымдамаларды практикалық бақылаулармен байланыстыруға көмектесе отырып, осы газ заңдарының принциптерін тиімді көрсетті.
Терминдер сөздігі
- Volume — Көлем
- Pressure — Қысым
- Temperature — Температура
- Heavy gas — Ауыр газ
- Light gas — Жеңіл газ
- Constant — Тұрақты шама