Закон идеального газа (уравнение Менделеева-Клапейрона)
Gas Properties by PhET Interactive Simulations, University of Colorado Boulder, licensed under CC-BY-4.0 (https://phet.colorado.edu)
Название проекта: Закон идеального газа (Уравнение Менделеева-Клапейрона)
Эта виртуальная лаборатория предназначена для использования на уроках химии по следующим темам:
- 10 класс. Глава VI. “Кинетика”.
Цели:
- изучить Закон идеального газа с помощью интерактивной симуляции PhET: Gas properties.
- объединить взаимосвязи из законов Бойля, Шарля и Гей-Люссака, для понимания Закона идеального газа (PV = nRT).
Теоретическая часть
Газовые законы описывают поведение газов в различных условиях. Понимание этих законов помогает нам предсказывать, как газы будут реагировать на изменения давления, объема или температуры.
Закон идеального газа
Закон идеального газа, также известный как уравнение Клапейрона-Менделеева, объединяет несколько простых газовых законов в одно уравнение:
PV = nRT
Это уравнение показывает, как связаны между собой давление (P), объем (V), количество частиц (n), газовая постоянная (R) и температура (T).
- P (давление) — это сила, которую частицы газа оказывают на стенки своего контейнера.
- V (объем) — это пространство, которое занимает газ.
- n (число молей) — это количество газа.
- R (газовая постоянная) — это фиксированное значение, которое делает единицы измерения корректными (8,31 Дж/(моль·К)).
- T (температура) — это мера скорости движения частиц газа.
Закон Бойля (P ∝ 1/V при постоянной T)
Закон Бойля утверждает, что при постоянной температуре давление и объем газа обратно пропорциональны. Это значит:
- Когда объем уменьшается, давление увеличивается.
- Когда объем увеличивается, давление уменьшается.
Уравнение: P₁V₁ = P₂V₂
Закон Шарля (V ∝ T при постоянном P)
Закон Шарля утверждает, что при постоянном давлении объем и температура газа прямо пропорциональны. Это значит:
- Когда температура увеличивается, объем увеличивается.
- Когда температура уменьшается, объем уменьшается.
Уравнение: V₁/T₁ = V₂/T₂
Закон Гей-Люссака (P ∝ T при постоянном V)
Закон Гей-Люссака утверждает, что при постоянном объеме давление и температура газа прямо пропорциональны. Это значит:
- Когда температура увеличивается, давление увеличивается.
- Когда температура уменьшается, давление уменьшается.
Уравнение: P₁/T₁ = P₂/T₂
Практическая часть

- Запустите симуляцию. Этот инструмент моделирует поведение газовых частиц в контейнере, помогая визуализировать такие концепции, как давление, объем и температура.
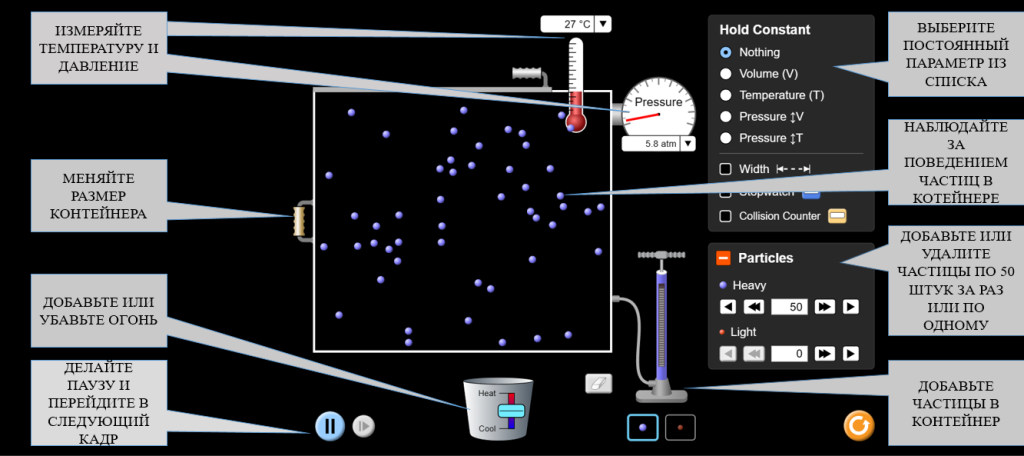
2.Ознакомьтесь с компонентами симуляции: система частиц (молекулы газа), контейнер и регулируемые параметры, такие как давление (P), объем (V) и температура (T).
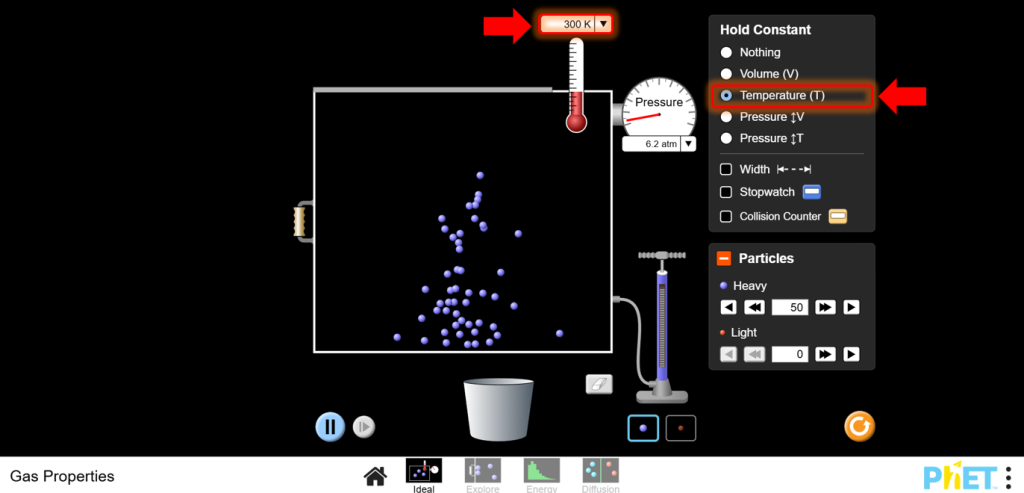
Исследование закона Бойля (P ∝ 1/V при постоянной T)
- Перейдите на экран Ideal в симуляции. Установите начальные условия: Начните с фиксированного количества частиц (N) и постоянной температуры (T). Вы будете наблюдать, как давление меняется с объемом.
4.Регулируйте объем:
a.Используйте левую стенку контейнера, чтобы изменить объем. Уменьшите объем и наблюдайте, как давление увеличивается.
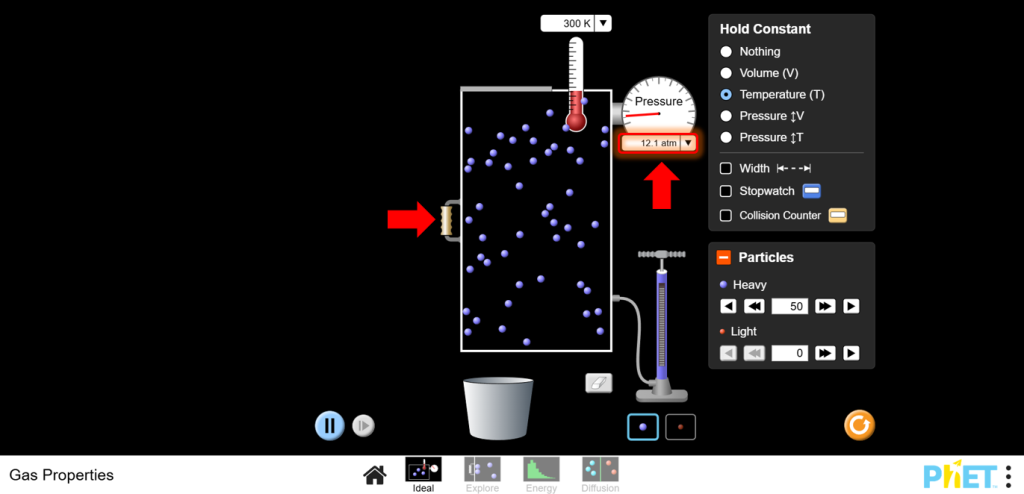
b.Увеличьте объем и наблюдайте, как давление уменьшается.
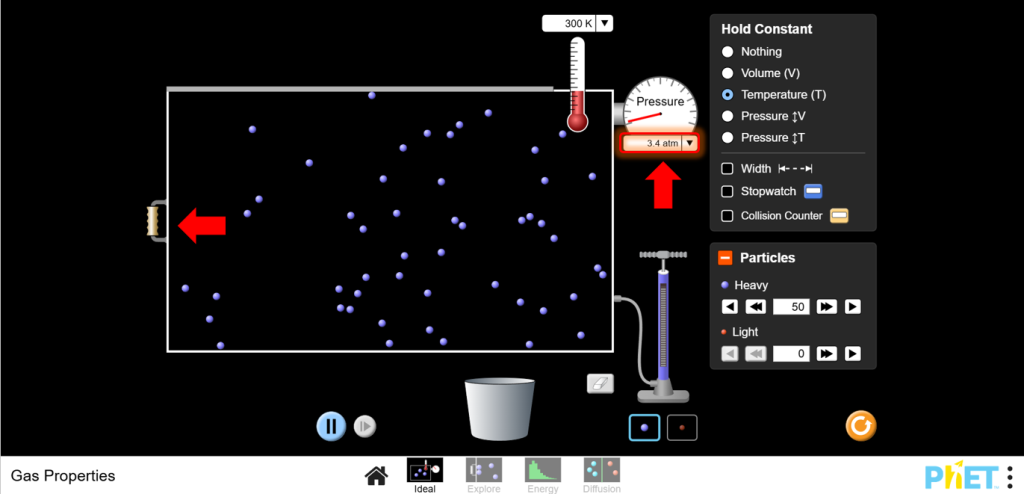
5. Обсуждение: Закон Бойля утверждает, что давление и объем обратно пропорциональны при постоянной температуре. Запишите свои наблюдения и постройте график P в зависимости от 1/V, чтобы увидеть обратную зависимость.
Исследование закона Шарля (V ∝ T при постоянном P)
- Настройка для закона Шарля:Перейдите на экран Ideal. Поддерживайте постоянное давление, при необходимости регулируя левую стенку контейнера.
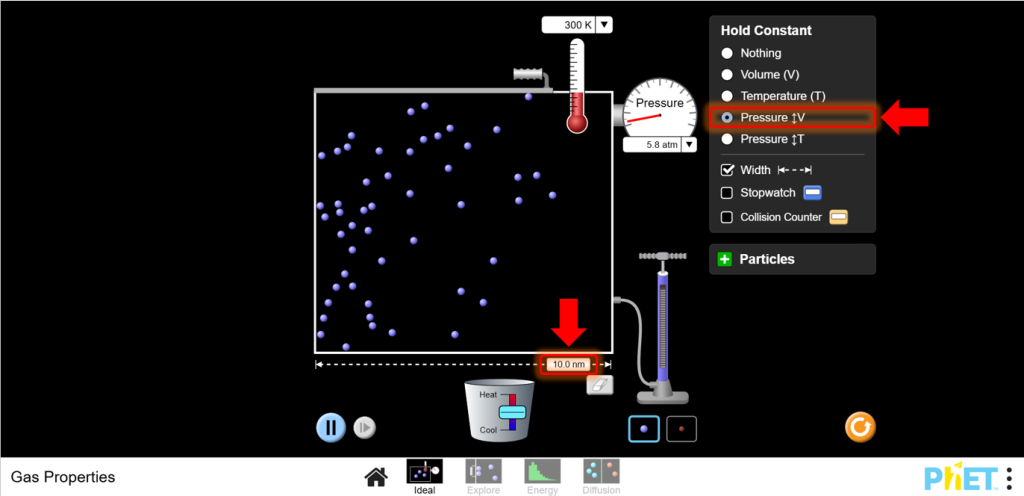
7. Меняйте температуру:
a.Увеличивайте температуру с помощью нагревателя. Обратите внимание, как объем контейнера изменяется с температурой. Наблюдайте, что при увеличении температуры объем увеличивается
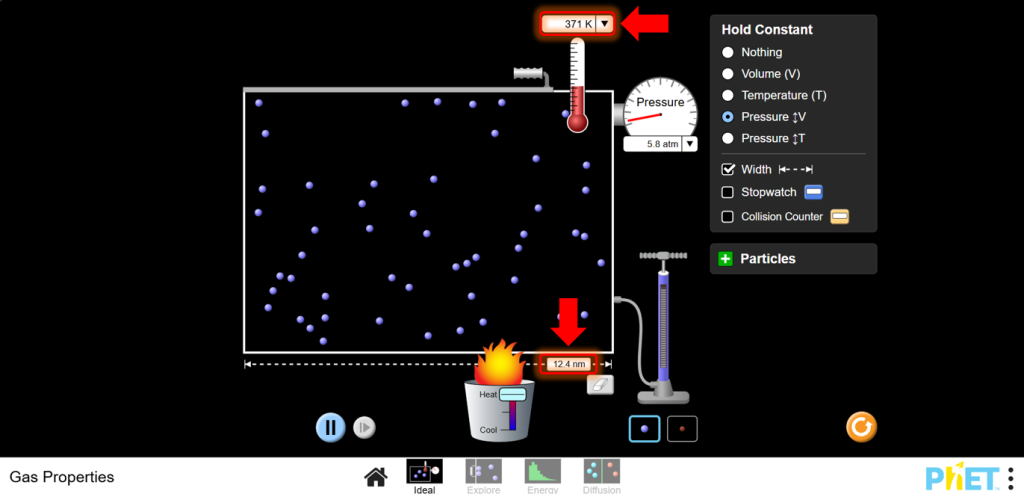
b. Уменьшайте температуру с помощью охладителя. Наблюдайте, что при уменьшении температуры объем уменьшается.
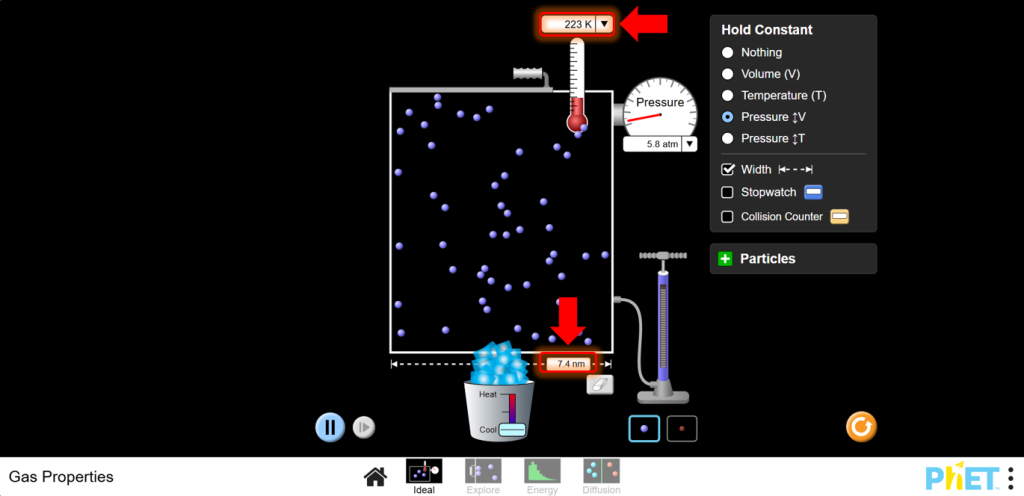
8.Обсуждение: Закон Шарля показывает прямую зависимость между температурой и объемом при постоянном давлении. Постройте график V в зависимости от T и наблюдайте линейную зависимость.
Исследование закона Гей-Люссака (P ∝ T при постоянном V)
- Настройка для закона Гей-Люссака: Продолжайте работу на экране Ideal. Поддерживайте постоянный объем, не регулируя левую стенку контейнера.
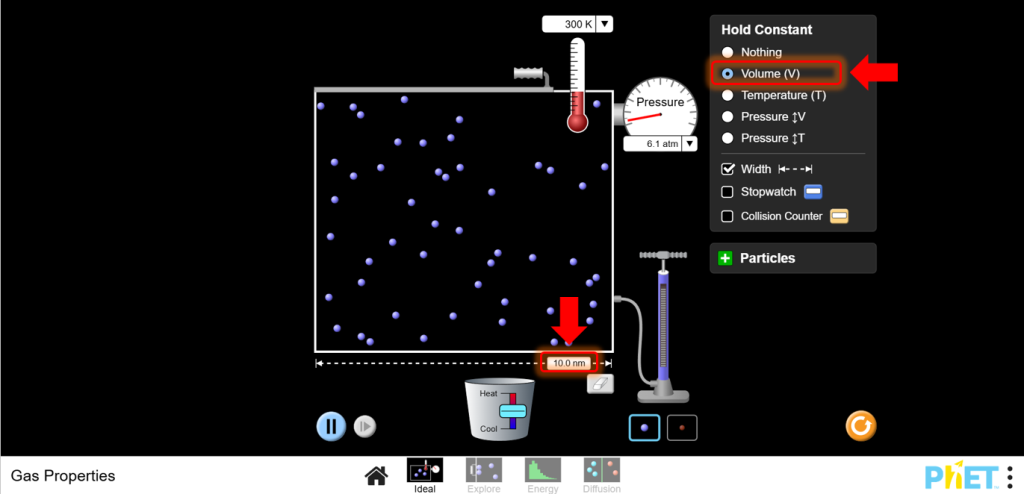
10. Меняйте температуру:
a. Используйте нагреватель, чтобы увеличить температуру. Следите за тем, как изменяется давление при изменении температуры. Вы должны увидеть, что при увеличении температуры давление увеличивается.
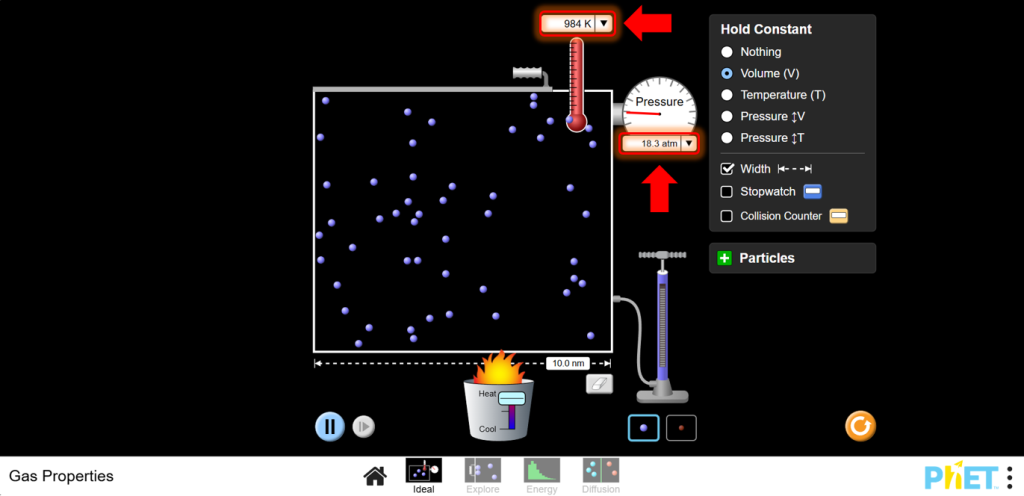
b.Используйте охладитель, чтобы уменьшить температуру. Вы должны увидеть, что при уменьшении температуры давление тоже уменьшается.
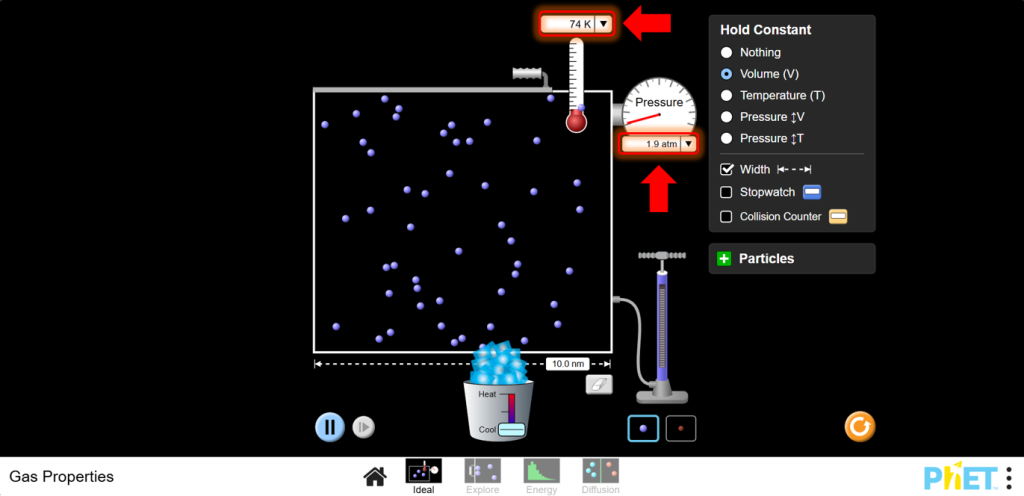
11. Обсуждение: Закон Гей-Люссака утверждает прямую зависимость между давлением и температурой при постоянном объеме. Постройте график P в зависимости от T, чтобы визуализировать эту прямую пропорциональность.
Применение закона идеального газа (PV = nRT)
- Исследуйте как законы Бойля, Шарля и Гей-Люссака объединяются в закон идеального газа.
- Проведите эксперимент:
a. Выберите фиксированное количество частиц.
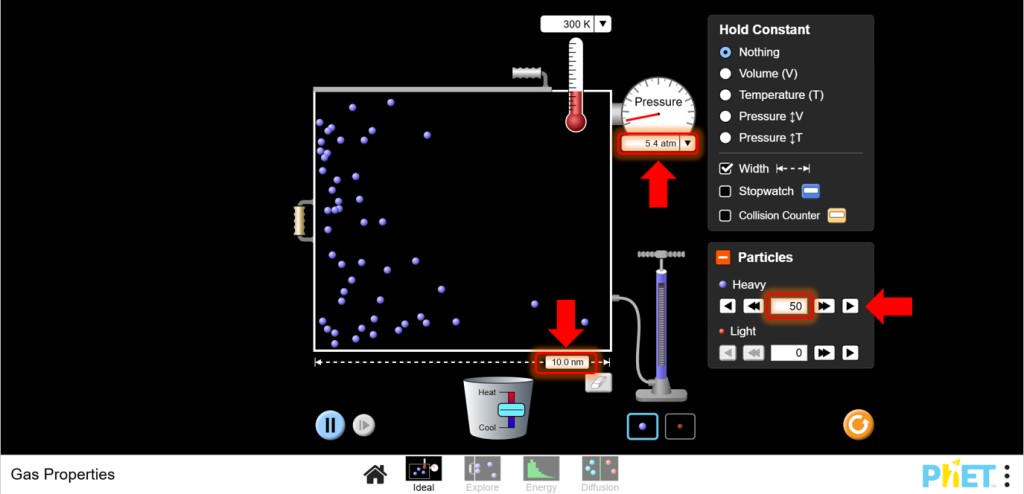
b. Регулируйте одну переменную (например, объем) и наблюдайте изменения давления и температуры. Предсказывайте изменения на основе закона идеального газа
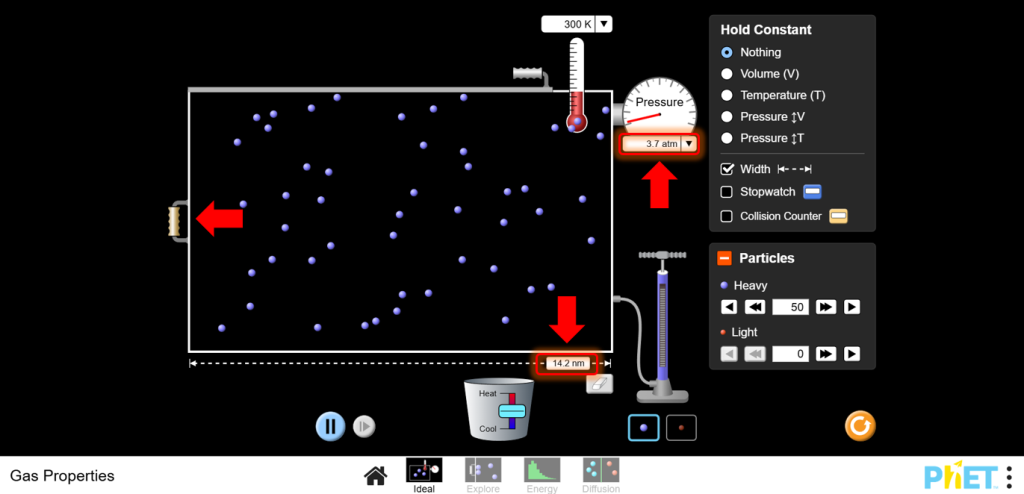
14. Практика расчетов: Вы можете поработать с различными сценариями, чтобы вычислить неизвестные величины, используя PV = nRT, укрепляя математическую связь.
Заключение
Использование симуляции PhET «Gas Properties» предоставило практический подход к изучению закона идеального газа и его составных частей: закона Бойля, закона Шарля и закона Гей-Люссака. Проводя интерактивные эксперименты, ученики смогли визуализировать и понять поведение газов в различных условиях. Симуляция эффективно продемонстрировала принципы этих газовых законов, помогая ученикам связать теоретические концепции с практическими наблюдениями.
Словарь терминов
- Volume — Объем
- Pressure — Давление
- Temperature — Температура
- Heavy gas — Тяжелый газ
- Light gas — Легкий газ
- Constant — Постоянная